Trong lĩnh vực sản xuất trang thiết bị y tế thì việc sản phẩm đạt chất lượng cũng là một trong những yêu cầu hàng đầu hiện nay để đảm bảo an toàn cho người bệnh. ISO 13485 ra đời chính là tiêu chuẩn quốc tế khắt khe về hệ thống quản lý chất lượng, được thiết kế chuyên biệt để đảm bảo an toàn và hiệu quả cho thiết bị y tế. Bộ tiêu chuẩn này tập trung chặt chẽ vào việc kiểm soát rủi ro, tuân thủ nghiêm ngặt các quy định pháp lý trong suốt quá trình sản xuất và cung ứng. Bài viết này, DiendanISO xin cung cấp những thông tin chi tiết về bộ tiêu chuẩn ISO 13485:2016 mới nhất và chuyên sâu.

Nội dung
- 1 ISO 13485 LÀ GÌ ?
- 2 Lịch sử phát triển bộ tiêu chuẩn ISO 13485
- 3 Video giới thiệu về Tiêu chuẩn ISO 13485
- 4 Đối tượng của ISO 13485:2016
- 5 Điểm nổi bật của bộ tiêu chuẩn ISO 13485:2016
- 6 Các nội dung cơ bản của tiêu chuẩn ISO 13485:2016
- 7 Lợi ích khi doanh nghiệp áp dụng ISO 13485:2016
- 8 Quy trình xây dựng ISO 13485:2016
- 8.1 Bước 1: Đánh giá hiện trạng và cam kết từ lãnh đạo
- 8.2 Bước 2: Thành lập Ban ISO và đào tạo nhận thức
- 8.3 Bước 3: Xác định phạm vi áp dụng và các bên liên quan
- 8.4 Bước 4: Xây dựng hệ thống tài liệu quản lý chất lượng (QMS)
- 8.5 Bước 5: Triển khai áp dụng vào thực tế
- 8.6 Bước 6: Đánh giá nội bộ và cải tiến liên tục
- 8.7 Bước 7: Rà soát của lãnh đạo (Management Review)
- 8.8 Bước 8: Chứng nhận ISO 13485 (nếu cần)
ISO 13485 LÀ GÌ ?
Tiêu chuẩn mới có tên đầy đủ là ISO 13485:2016 – Hệ thống quản lý An toàn cho sản phẩm Y Tế. ISO 13485 đưa ra các yêu cầu đối với hệ thống quản lý chất lượng áp dụng tại các cơ sở sản xuất, kinh doanh dụng cụ y tế. Tiêu chuẩn ISO 13485 đảm bảo khả năng cung cấp sản phẩm đáp ứng yêu cầu của khách hàng và các quy định của luật pháp.
Trong lĩnh vực sản xuất trang thiết bị y tế, việc áp dụng hệ thống quản lý chất lượng không còn là lựa chọn mà đã trở thành yêu cầu bắt buộc theo quy định pháp luật hiện hành. Trước đây, theo Nghị định 36/2016/NĐ-CP, các doanh nghiệp được yêu cầu hoàn thành việc áp dụng ISO 13485 trước ngày 01/01/2020 trong giai đoạn chuyển tiếp.
Tuy nhiên, đến nay quy định này đã được thay thế và cập nhật bởi Nghị định 98/2021/NĐ-CP. Theo đó, các cơ sở sản xuất trang thiết bị y tế bắt buộc phải xây dựng, áp dụng và duy trì hệ thống quản lý chất lượng theo tiêu chuẩn ISO 13485:2016 nhằm đảm bảo kiểm soát chặt chẽ quy trình sản xuất, nâng cao chất lượng sản phẩm và đáp ứng yêu cầu quản lý của cơ quan chức năng.

Có thể thấy được bộ tiêu chuẩn ISO 13485:2016 này hiện là tiêu chuẩn quốc tế mới nhất dành riêng cho ngành thiết bị y tế, giúp doanh nghiệp chuẩn hóa quy trình, kiểm soát rủi ro, nâng cao hiệu suất vận hành và tăng khả năng hội nhập thị trường toàn cầu. Việc tổ chức, doanh nghiệp tuân thủ đầy đủ các yêu cầu của bộ tiêu chuẩn này không chỉ đảm bảo yêu cầu pháp lý mà còn là yếu tố quan trọng giúp doanh nghiệp xây dựng uy tín, nâng cao năng lực cạnh tranh và phát triển bền vững trong ngành y tế.
Lịch sử phát triển bộ tiêu chuẩn ISO 13485
ISO 13485 là hệ thống quản lý chất lượng quốc tế dành riêng cho ngành thiết bị y tế. Để áp dụng thành công, doanh nghiệp cần nắm rõ lộ trình phát triển của các phiên bản sau:

- ISO 13485:2003
Nền tảng đầu tiên: Được ban hành vào tháng 7/2003, đây là phiên bản đặt nền móng cho quản lý an toàn sản phẩm y tế (tương đương với TCVN ISO 13485:2004 tại Việt Nam).
- ISO 13485:2012 (hay BS EN ISO 13485:2012):
Cập nhật thị trường Châu Âu: Xuất phát từ những yêu cầu pháp quy khắt khe của Ủy ban Châu Âu, phiên bản này (hay BS EN ISO 13485:2012) đã sửa đổi các Phụ lục ZA, ZB, ZC để phù hợp với các Chỉ thị thiết bị y tế, trong khi nội dung cốt lõi vẫn được giữ nguyên.
Kết quả là CEN quyết định xuất bản một ấn bản mới của tiêu chuẩn (EN ISO 13485:2012). Tiêu chuẩn này có một Lời nói đầu được sửa đổi và các Phụ lục ZA, ZB và ZC, nhưng văn bản cốt lõi vẫn không thay đổi.
- ISO 13485:2016 – Phiên bản mới nhất
Tiêu chuẩn vàng hiện hành: Ra mắt ngày 01/03/2016, đây là phiên bản mới nhất thay thế hoàn toàn tiền nhiệm 2003. Với sự chuyển đổi nghiêm ngặt kết thúc vào năm 2019, ISO 13485:2016 hiện là thước đo uy tín bắt buộc để doanh nghiệp y tế khẳng định chất lượng trên toàn cầu.
Tại Diễn đàn ISO, chúng tôi liên tục cập nhật những kiến thức chuyên sâu nhất về lộ trình áp dụng và các thay đổi trọng yếu của bộ tiêu chuẩn này.
Nguồn tham khảo: iso.org, tcvn.gov.vn
Video giới thiệu về Tiêu chuẩn ISO 13485
Đối tượng của ISO 13485:2016
Với bộ tiêu chuẩn ISO 13485:2016 này có thể được áp dụng cho tất cả các tổ chức tham gia vào vòng đời của thiết bị y tế và các dịch vụ có liên quan. Những doanh nghiệp đó có thể là:
- Doanh nghiệp sản xuất trang thiết bị y tế: Các tổ chức trực tiếp thiết kế, sản xuất và cung cấp thiết bị y tế ra thị trường.
- Đơn vị gia công, lắp ráp: Các tổ chức tham gia một phần hoặc toàn bộ quá trình sản xuất theo hợp đồng.
- Doanh nghiệp phân phối và kinh doanh thiết bị y tế: Các đơn vị nhập khẩu, phân phối hoặc bán thiết bị y tế.
- Tổ chức cung cấp dịch vụ liên quan: Bao gồm bảo trì, sửa chữa, hiệu chuẩn thiết bị y tế.
- Doanh nghiệp cung cấp linh kiện, vật tư: Các nhà cung cấp tham gia vào chuỗi cung ứng sản xuất thiết bị y tế.
- Tổ chức tư vấn, thiết kế và phát triển sản phẩm y tế.

Việc áp dụng ISO 13485:2016 giúp các tổ chức trong ngành y tế đảm bảo sản phẩm đáp ứng yêu cầu an toàn, chất lượng và tuân thủ quy định pháp luật, đồng thời nâng cao uy tín và khả năng cạnh tranh trên thị trường trong nước và quốc tế.
Điểm nổi bật của bộ tiêu chuẩn ISO 13485:2016
Xét về bản chất, ISO 13485:2016 có thể được xem là một hệ thống quản lý chất lượng chuyên biệt, được phát triển dựa trên nền tảng của ISO 9001 nhưng áp dụng riêng cho các tổ chức hoạt động trong lĩnh vực trang thiết bị y tế như thiết kế, sản xuất, lắp đặt và bảo trì. Tuy nhiên, tiêu chuẩn này được bổ sung thêm nhiều yêu cầu khắt khe nhằm đảm bảo mức độ an toàn và kiểm soát cao hơn.
Thông thường, các tiêu chuẩn ISO hiện đại được xây dựng theo cấu trúc cấp cao (High-Level Structure – HLS) để đảm bảo tính đồng bộ và dễ tích hợp giữa các hệ thống quản lý. Tuy nhiên, ISO 13485:2016 không áp dụng hoàn toàn cấu trúc HLS do tính đặc thù của ngành y tế. Thay vào đó, tiêu chuẩn này được xây dựng dựa trên 5 yếu tố cốt lõi, kế thừa từ cấu trúc của ISO 9001 nhưng có điều chỉnh để phù hợp hơn với yêu cầu kiểm soát thiết bị y tế.
1. Tập trung vào an toàn và hiệu quả của thiết bị y tế
Khác với ISO 9001 (tập trung vào sự hài lòng của khách hàng), bộ tiêu chuẩn ISO 13485 lại có ưu tiên đảm bảo thiết bị y tế an toàn và hoạt động hiệu quả trong suốt vòng đời sản phẩm.

2. Kiểm soát rủi ro trong toàn bộ vòng đời sản phẩm
Tiêu chuẩn yêu cầu tích hợp hoạt động quản lý rủi ro vào tất cả các giai đoạn, từ thiết kế, sản xuất đến phân phối và hậu mãi, dựa trên nguyên tắc của ISO 14971.
3. Kiểm soát chặt chẽ quy trình sản xuất và nhà cung cấp
Bộ tiêu chuẩn này yêu cầu việc kiểm soát tài liệu, hồ sơ, quy trình sản xuất và đánh giá, lựa chọn và theo dõi nhà cung cấp dựa trên rủi ro và mức độ ảnh hưởng đến chất lượng sản phẩm.
4. Quản lý thiết kế và phát triển sản phẩm
Thiết lập quy trình rõ ràng để kiểm soát thiết kế từ yêu cầu ban đầu, thử nghiệm, xác nhận (validation), đến thay đổi thiết kế.
5. Giám sát sau sản xuất & phản hồi từ thị trường (Post-Market Surveillance)
ISO 13485 yêu cầu tổ chức phải có cơ chế ghi nhận, phân tích và phản hồi các thông tin sau khi sản phẩm ra thị trường, như:
- Khiếu nại khách hàng
- Sự cố, lỗi sản phẩm
- Hoạt động triệu hồi thiết bị (nếu cần)
Những yếu tố này giúp ISO 13485:2016 trở thành tiêu chuẩn cốt lõi, đảm bảo chất lượng và an toàn cho thiết bị y tế, đồng thời nâng cao năng lực quản lý và uy tín của doanh nghiệp trên thị trường.
Các nội dung cơ bản của tiêu chuẩn ISO 13485:2016
ISO 13485:2016 bao gồm 08 Điều khoản. 03 Điều khoản đầu tiên là khái quát, định nghĩa, giải thích. 05 Điều khoản còn lại là các yêu cầu cốt lõi của ISO 13485: 2016.
Dưới đây là giới thiệu chung về các Điều khoản. Để áp dụng điều khoản này vào thực tế. Doanh nghiệp cần thêm nhiều thông tin và kinh nghiệp. Doanh nghiệp có thể tham khảo bài viết của chúng tôi dưới đây để có thể áp dụng.
Các yêu cầu cơ bản của ISO 13485:2016 bao gồm:
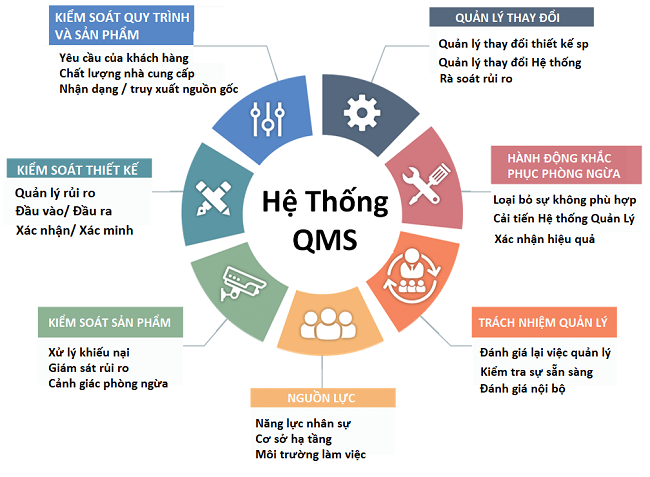
|
Điều Khoản |
Nội Dung |
Yêu Cầu |
| Điều khoản 4: Hệ thống quản lý chất lượng |
Điều khoản 4 thiết lập các yêu cầu chung cho một hệ thống QLCL bao gồm tài liệu hệ thống và thông tin về hồ sơ. |
Điều khoản 04 yêu cầu:
|
| Điều khoản 5: Trách nhiệm lãnh đạo |
Đây là nơi lãnh đạo sẽ tìm thấy các yêu cầu trách nhiệm của họ để thực hiện và duy trì QMS. Lãnh đạo cần lập kế hoạch và đánh giá liên tục để đảm bảo QMS đang hoạt động tốt. |
Điều khoản 5 yêu cầu:
|
| Điều khoản 6: Quản lý nguồn lực của Doanh nghiệp |
Phần này tương đối ngắn, nhưng nó bao gồm mọi thứ về kiểm soát và quản lý nguồn lực của Doanh nghiệp. Bao gồm nhân sự, máy móc thiết bị, cơ sở hạ tầng và môi trường làm việc. |
Điều khoản 6 yêu cầu:
|
| Điều khoản 7: Quá trình tạo sản phẩm |
Các yêu cầu cụ thể của sản phẩm bao gồm từ việc thiết kế (hoặc dịch vụ) và sản xuất các thiết bị y tế. |
Điều khoản 07 yêu cầu:
|
|
Điều khoản 8: Đo lường, phân tích và cải tiến |
Điều khoản 8 đưa ra các yêu cầu để đảm bảo Doanh nghiệp có thể hiểu QMS của họ hoạt động như thế nào. Có điểm nào không phù hợp, cần cải tiến hay không. Điều này bao gồm các hành động khắc phục và phòng ngừa; Đánh giá sự hài lòng của khách hàn; Kiểm soát sự không phù hợp của sản phẩm; Đánh giá và cải thiện các chính sách và quy trình chất lượng; Thực hiện xem xét về đánh giá nội bộ và cải tiến liên tục hệ thống. |
Điều khoản 8 yêu cầu:
|
Lợi ích khi doanh nghiệp áp dụng ISO 13485:2016
Hiện nay các tổ chức, doanh nghiệp hoạt động trong lĩnh vực trang thiết bị y tế đang áp dụng bộ tiêu chuẩn ISO 13485:2016 này khá nhiều. Đây vừa là một yêu cầu cũng như một xu hướng chung để hướng đến chuẩn mực quốc tế và đảm bảo chất lượng sản phẩm họ làm ra. Những lợi ích thiết thực được thể hiện như sau:
1. Đảm bảo an toàn và hiệu quả thiết bị y tế
ISO 13485 giúp doanh nghiệp kiểm soát chất lượng toàn diện, đảm bảo sản phẩm an toàn cho người sử dụng và đáp ứng các yêu cầu kỹ thuật trong suốt vòng đời.
2. Tuân thủ quy định pháp lý và điều kiện thị trường
Áp dụng ISO 13485 giúp doanh nghiệp đáp ứng yêu cầu của các cơ quan quản lý y tế (FDA – Hoa Kỳ, CE – Châu Âu, TBYT Việt Nam…), tạo điều kiện thuận lợi để doanh nghiệp xin giấy phép lưu hành sản phẩm cũng như mở rộng thị trường xuất khẩu.

3. Tăng cường uy tín và niềm tin từ khách hàng
Có chứng nhận ISO 13485 chứng minh doanh nghiệp vận hành hệ thống quản lý chất lượng nghiêm ngặt, qua đó:
- Tăng uy tín với đối tác, bệnh viện, người tiêu dùng
- Giành lợi thế trong đấu thầu và hợp tác quốc tế
4. Cải thiện hiệu quả quy trình và giảm chi phí
Việc kiểm soát rủi ro, tài liệu, và nhà cung cấp giúp cho tổ chức giảm lãng phí và sai lỗi của sản phẩm. Bên cạnh đó còn hạn chế sự cố cần triệu hồi cũng như tối ưu hóa hiệu quả sản xuất.
5. Tăng khả năng kiểm soát và truy xuất nguồn gốc
Mỗi lô sản phẩm, linh kiện, và quy trình đều được ghi nhận và kiểm soát. Bên cạnh đó còn hỗ trợ cho việc truy xuất nhanh và chính xác trong các tình huống cần điều tra sự cố.
6. Thúc đẩy cải tiến liên tục
Tiêu chuẩn yêu cầu phải liên tục đánh giá nội bộ, theo dõi dữ liệu hiệu suất, và hành động khắc phục phòng ngừa, từ đó giúp nâng cao chất lượng sản phẩm và tăng năng suất cũng như cải thiện hoạt động của doanh nghiệp.
Quy trình xây dựng ISO 13485:2016
Để triển khai hiệu quả hệ thống quản lý chất lượng theo ISO 13485:2016, doanh nghiệp cần xây dựng một lộ trình rõ ràng, bài bản và phù hợp với thực tế vận hành. Quy trình áp dụng tiêu chuẩn thường được thực hiện theo các bước sau:
-
Bước 1: Đánh giá hiện trạng và cam kết từ lãnh đạo
Doanh nghiệp tiến hành khảo sát toàn bộ hoạt động hiện tại nhằm xác định mức độ đáp ứng so với yêu cầu của ISO 13485. Đồng thời, ban lãnh đạo cần thể hiện cam kết mạnh mẽ thông qua việc phân bổ nguồn lực, ngân sách và định hướng triển khai hệ thống.
-
Bước 2: Thành lập Ban ISO và đào tạo nhận thức
Tổ chức thành lập Ban ISO 13485 với sự tham gia của các bộ phận chủ chốt. Song song đó, cần triển khai các chương trình đào tạo nhằm nâng cao nhận thức về tiêu chuẩn ISO 13485 và các nguyên tắc quản lý chất lượng trong lĩnh vực trang thiết bị y tế.

-
Bước 3: Xác định phạm vi áp dụng và các bên liên quan
Doanh nghiệp cần xác định rõ phạm vi áp dụng hệ thống (như thiết kế, sản xuất, phân phối, hậu mãi…). Đồng thời, phân tích yêu cầu của các bên liên quan như khách hàng, cơ quan quản lý, nhà cung cấp để đảm bảo tuân thủ đầy đủ.
-
Bước 4: Xây dựng hệ thống tài liệu quản lý chất lượng (QMS)
Tiến hành thiết lập và chuẩn hóa bộ tài liệu bao gồm: chính sách và mục tiêu chất lượng, sổ tay chất lượng, quy trình vận hành, hướng dẫn công việc và các biểu mẫu liên quan. Tài liệu cần được thiết kế phù hợp với đặc thù sản phẩm và mô hình hoạt động của doanh nghiệp.
-
Bước 5: Triển khai áp dụng vào thực tế
Đưa hệ thống vào vận hành thông qua việc áp dụng các quy trình đã xây dựng trong hoạt động hằng ngày. Doanh nghiệp cần tổ chức đào tạo, hướng dẫn nhân sự và thực hiện giám sát định kỳ để đảm bảo tuân thủ.
-
Bước 6: Đánh giá nội bộ và cải tiến liên tục
Thực hiện đánh giá nội bộ định kỳ nhằm phát hiện các điểm chưa phù hợp. Từ đó, doanh nghiệp đưa ra hành động khắc phục và phòng ngừa, đồng thời cập nhật, cải tiến hệ thống để nâng cao hiệu quả vận hành và duy trì sự phù hợp với tiêu chuẩn ISO 13485:2016.

Bước 7: Rà soát của lãnh đạo (Management Review)
Ban giám đốc đánh giá toàn bộ hệ thống QMS: các hiệu quả hoạt động cũng như tình trạng cải tiến, hành động khắc phục và mức độ thỏa mãn khách hàng và bên liên quan
Bước 8: Chứng nhận ISO 13485 (nếu cần)
Doanh nghiệp của bạn cần lựa chọn tổ chức chứng nhận uy tín để đến đánh giá và cấp chứng nhận cho doanh nghiệp. Thông thường khi tổ chức chứng nhận đến sẽ trải qua 2 giai đoạn đánh giá bao gồm:
- Giai đoạn 1: kiểm tra tài liệu và sự sẵn sàng
- Giai đoạn 2: đánh giá thực tế tại hiện trường
Nhận giấy chứng nhận nếu đạt yêu cầu
Hy vọng những kiến thức trên đây mà diendaniso cung cấp đã giúp bạn hiểu hơn về Hệ thống Quản Lý Trang Thiết Bị Y Tế ISO 13485:2016 ! Mọi thông tin trong bài viết mang tính tham khảo. Độc giả nên liên hệ chuyên gia tư vấn để áp dụng phù hợp theo từng loại hình doanh nghiệp.











































 Messenger
Messenger Zalo
Zalo